VERTIGINI di Kai S. Paulus

(Pillola n. 74)
Un anno fa ci siamo occupati di vertigini (PARKINSON ESTIVO: CAPOGIRI E VERTIGINI) che, specialmente nel periodo estivo, possono creare importanti disagi nelle persone affette da malattia di Parkinson, perché l’effetto ipotensivo del caldo si somma a quello dei farmaci e della malattia stessa. Ed abbiamo visto che l’antidoto può essere semplicemente bere più acqua.
Ma che cosa sono esattamente le vertigini e dove originano?
Le vertigini sono espressione di una alterazione del sistema dell’equilibrio.
Il sistema dell’equilibrio ci permette di contrastare la forza di gravità, di stare in piedi e di muoverci.
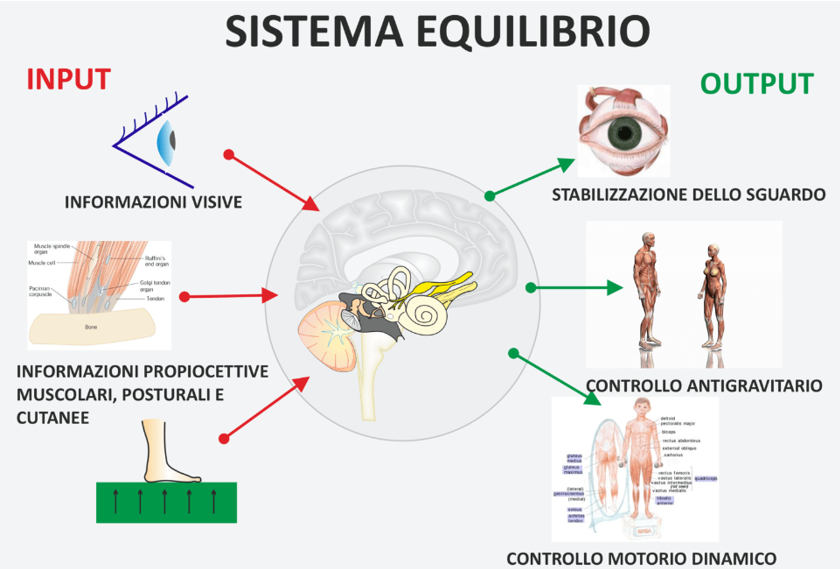
Il sistema dell’equilibrio è costituito dai sistemi sensoriali, visivo, uditivo, propriocettivo e tattile, che informano il cervello in ogni istante della nostra posizione; ed il cervello può mantenere l’equilibrio, correggere posture errate, o prepararci al movimento, integrando l’informazione visiva (la vista è uno strumento formidabile di orientamento; in effetti al buio si sbanda) con quella propriocettiva e tattile (muscoli, tendini e cute informano il cervello sul contatto del corpo a pavimento, sedia, letto, ecc). Ovviamente, le informazioni devono essere congrue, diversamente il sistema non riesce ad integrare correttamente le diverse informazioni sensoriali.

Per esempio, se ci si sporge da una altezza e si guarda in basso, il sistema propriocettivo e tattile informa il cervello che il corpo appoggia a circa 90 cm, mentre la vista rivela una distanza di diversi metri; questa discrepanza viene percepita come errata e si percepiscono le vertigini.
Oppure, all’interno dell’orecchio si trovano i canali semicircolari, tre per lato, per ogni dimensione dello spazio. Questi canali fungono un po’ come delle livelle e che devono sempre essere allineate. Se un canale è danneggiato (trauma, infezione, ecc.), quello controlaterale prende il sopravento ed il cervello lo registra come cambio di direzione, che però non è avvenuto, quindi disequilibrio e quindi vertigini. Oppure, in un canale si staccano degli otoliti (che servono da contrappeso nei canali semicircolari) e che vagano senza controllo nei canali stimolando il nervo vestibolare come se ci si fosse mossi, ma non c’è stato nessun movimento, quindi disequilibrio e vertigini.
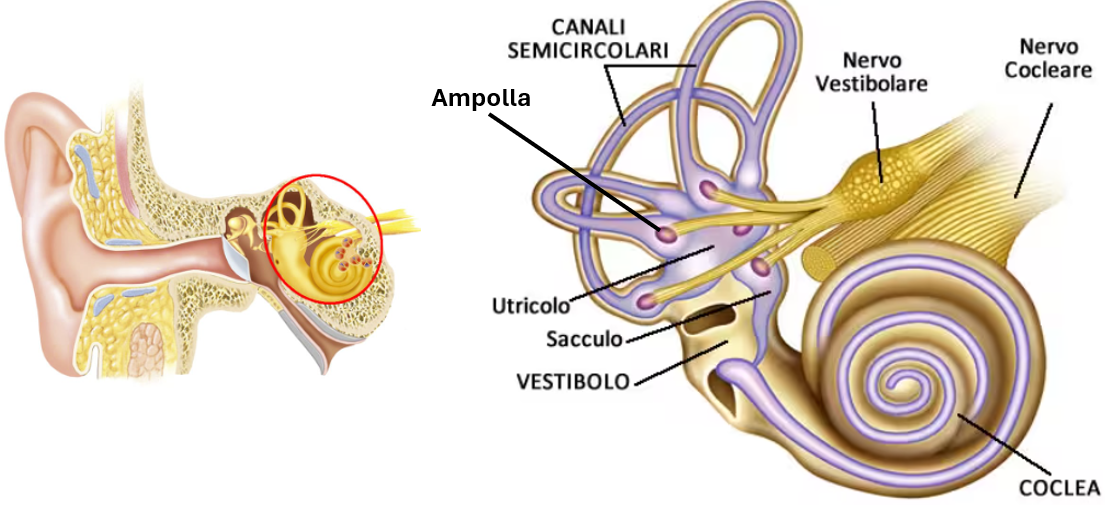
A sinistra: anatomia dell’orecchio esterno ed interno; a destra: l’orecchio interno suddiviso in coclea e nervo cocleare per l’udito, ed il sistema vestibolare con i canali semicircolari e nervo vestibolare, responsabili per l’equilibrio.
Le cause delle vertigini sono tantissime: età, altezze, dislivelli, alterazioni dell’udito, della vista, della postura, infezioni, malattie cardiocircolatorie, dismetaboliche (diabete), e neurodegenerative (come il Parkinson), ma anche elevate temperature estive e farmaci.
Che cosa possiamo fare?
Il caldo ovviamente si combatte con il refrigerio e con l’acqua, le malattie che possono causare vertigini vanno trattate correttamente, farmaci che possono dare problemi vanno evitate, ed infine, il disequilibrio si cura con il miglioramento dell’equilibrio statico-dinamico con il movimento, il ballo e la riabilitazione neuromotoria.
Fonti bibliografiche:
Dlugariczyk J. “Schwierige” Patient:innen – Vestibularisdiagnostik unter erschwerten Bedingungen: Teil 2. HNO, 2024; 72: 129-140.
Li X, Wei C, Gao X, Sun J, Yang J. Global trends in the research on older population dizziness/vertigo: a 20-year bibliometric and visualization analysis. Braz J Otorhinolaryngol, 2024; 90(5): doi: 10.1016/j.bjorl.2024.101441.
Zwergal A, Lehner L, Goldschagg, Strupp M. Akuter, episodischer und chronischer zentraler Schwindel – differenzialdiagnosen kenn, richtig behandeln. DNP Neurologie & Psychiatrie, 2024; 25(3): 55-65.

Copertina di una mia recente lezioni sulle vertigini per il corso regionale di formazione dei medici di medicina generale.