CONOSCERE “SU NEMIGU” di Kai S. Paulus

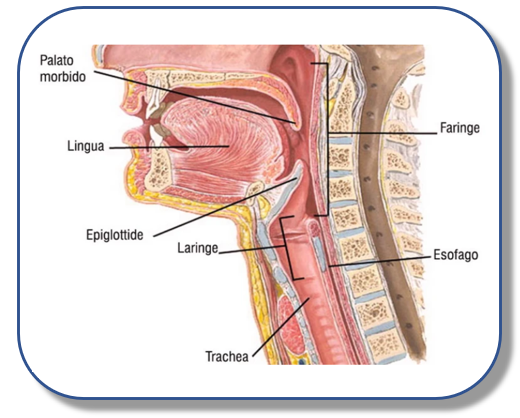
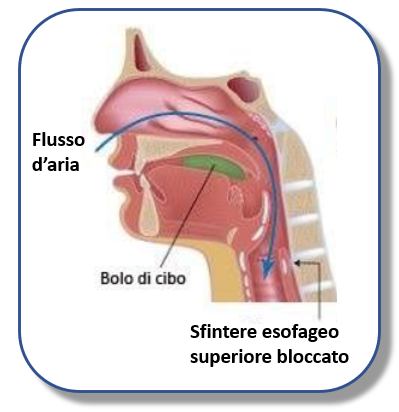
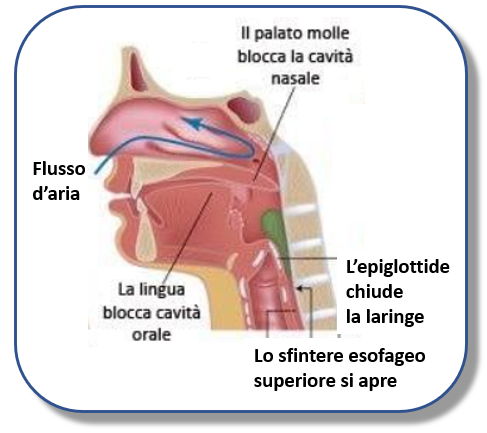
(Il Tempio Greco: La Rampa)
[All’inizio del nostro Progetto “Il Tempio Greco” abbiamo parlato dell’accettazione della malattia come prerogativa necessaria per poter comprendere e affrontare le tante problematiche del Parkinson, e quindi l’accettazione rappresenta le fondamenta del nostro Tempio (vedi “ CREPIDOMA: ACCETTAZIONE DELLA MALATTIA“ e “ STILOBATE: ACCETTAZIONE DELLA MALATTIA 2“). E pertanto riprendiamo la costruzione del Tempio anteponendo il capitolo della conoscenza, una specie di Rampa d’accesso al nostro Tempio, perché ritengo che, se conosco il mio avversario, lo temo di meno e quindi potrò contrastarlo meglio]
Ieri pomeriggio ci siamo incontrati nella nostra Casa Park in via Ardara a Sassari per il primo di una serie di appuntamenti di un nuovo progetto, quello di conoscere meglio la malattia di Parkinson, quel rapace infingardo, su nemigu.
In questo primo incontro abbiamo affrontato la storia, e cioè di come James Parkinson ha raccolto le sue osservazioni in un libretto “The shaking palsy” (La paralisi agitante, 1817) dando il via a “la malattia di Parkinson”, che poi non fu neanche lui a coniare questo termine, ma lo scienziato francese Jean-Martin Charcot che si riferiva, circa 40 anni dopo la pubblicazione de ‘La paralisi agitante’, alla malattia “di quel Parkinson” in una delle sue lezioni su persone rallentate e con tremore.
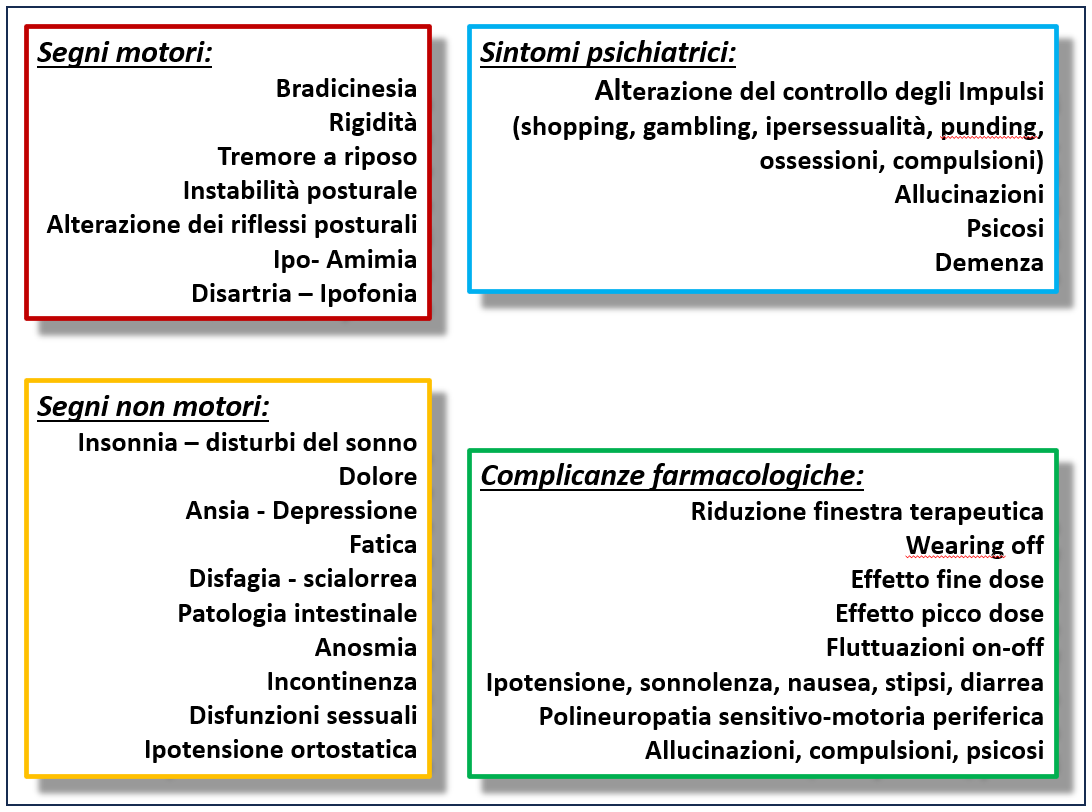
Ci siamo quindi occupati del quadro clinico ed abbiamo appreso che i sintomi e segni del Parkinson possono essere distinti in
1) segni motori, che sono quelli classici, come il tremore, il rallentamento motorio e la rigidità muscolare che generalmente rispondono alla terapia anti-Parkinson dopaminergica,

2) segni non motori, quali l’insonnia, i dolori e la depressione, che necessitano di farmaci specifici,

3) i sintomi psichiatrici (disinibizione, compulsioni, ossessioni, ecc.) che ovviamente vanno trattati separatamente ma anche con l’ottimizzazione della terapia farmacologica, ed infine

4) le complicazioni farmacologiche, causate proprio dagli stessi farmaci, che servono per far star meglio la persona ammalata, ma che possono provocare degli effetti spiacevoli e che rendono la gestione globale ulteriormente difficile.

Successivamente abbiamo affrontato i segni prodromici, cioè i sintomi che possono precedere per molti anni l’esordio vero e proprio del Parkinson, e che oggi rivestono enorme importanza perché possono aiutare a fare diagnosi preclinica, a intraprendere dei percorsi preventivi che, anche se non possono evitare la malattia, possono comunque ritardarla e magari rendere il suo decorso meno grave.

La cura di tali prodromi, quando presenti durante il Parkinson, è invece importante, per la sua gestione globale e per mantenere sufficienti autonomie e qualità di vita.
E’ importante sottolineare, che la presenza di uno di questi segni non è assolutamente indicativo per un Parkinson, e che, per esempio, la riduzione dell’olfatto è dovuta verosimilmente ad un raffreddore oppure ad una patologia otorinolaringoiatrica; oppure, la stitichezza può essere ricondotto ad una alimentazione non equilibrata; o ancora, si può essere tristi per una perdita o una delusione. Ovviamente in questi casi non pensiamo minimamente ad una malattia neurodegenerativa. Invece, i prodromi che potrebbero farci pensare ad un Parkinson sono quelli che si presentano per lunghi tempi, anche molti anni, ed apparentemente senza cause note.
Vorrei ringraziare il nostro ‘webmaster’ Gian Paolo Frau ed il nostro ‘fac totum’ Antonello Soro, senza i quali non saremo riusciti a tenere questa impegnativa lezione nella nostra bellissima nuova sede.
La prossima volta ci occuperemo delle cause di Parkinson, dove esattamente inizia nel nostro corpo, ed anche del perché. Ne vedremo delle belle!
Progetto “Il Tempio Greco – Le Sei Colonne del Parkinson”.
Sinora pubblicati: (cliccare sul titolo celeste per visualizzare l’articolo)
TEMPIO GRECO: CAMBIAMENTO PROGETTO
CREPIDOMA: ACCETTAZIONE DELLA MALATTIA
STILOBATE: ACCETTAZIONE DELLA MALATTIA 2
COLONNA DEL PARKINSON: I FARMACI
COLONNA DEL PARKINSON: TERAPIE AVANZATE
COLONNA DEL PARKINSON: LA RIABILITAZIONE
LA RIABILITAZIONE NEL TEMPIO DEL PARKINSON di Pinuccia Sanna
RIABILITAZIONE E DANZA di Annalisa Mambrini
COLONNA DEL PARKINSON: LA DISFAGIA
COLONNA DEL PARKINSON: LA DISFAGIA (2)
COLONNA DEL PARKINSON: LA DISFAGIA (3)
COLONNA DEL PARKINSON: INTERFACCIA CERVELLO – COMPUTER
COLONNA DEL PARKINSON: INTERFACCIA CERVELLO – COMPUTER (2)
![]()